摘要:研究發(fā)現(xiàn),人體在進(jìn)食后調(diào)節(jié)血糖的能力方面出現(xiàn)了一個(gè)令人驚訝的新參與者
最近的一項(xiàng)研究發(fā)表于Life Metabolism發(fā)現(xiàn)了一個(gè)令人驚訝的新參與者,即身體在進(jìn)食后調(diào)節(jié)血糖的能力。
貝勒醫(yī)學(xué)院和納穆爾大學(xué)的研究人員發(fā)現(xiàn),一種名為透明質(zhì)酸酶-1(HYAL1)的酶在抑制肝臟過度葡萄糖生成方面發(fā)揮著至關(guān)重要的作用,尤其是在飯后。這一發(fā)現(xiàn)可能為治療代謝紊亂打開了新的大門,如2型糖尿病,血糖控制受損。
 圖1 透明質(zhì)酸酶-1介導(dǎo)餐后肝糖異生的抑制
圖1 透明質(zhì)酸酶-1介導(dǎo)餐后肝糖異生的抑制這項(xiàng)研究的重點(diǎn)是透明質(zhì)酸(HA),這是一種在進(jìn)食后血液中自然涌動(dòng)的糖分子。雖然HA以其在組織結(jié)構(gòu)和炎癥這項(xiàng)研究揭示了其與葡萄糖代謝的意外聯(lián)系。該團(tuán)隊(duì)發(fā)現(xiàn),HYAL1能夠分解肝臟中的HA,有助于阻止葡萄糖異生——肝臟從非碳水化合物來源產(chǎn)生葡萄糖的過程。正常情況下,餐后糖異生被抑制以防止血糖飆升,但在糖尿病患者中,糖異生仍然過度活躍。
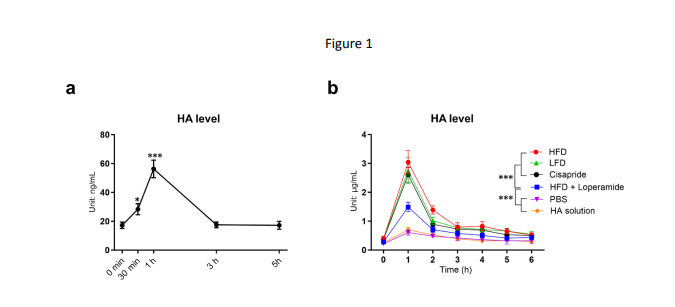
圖2 餐后循環(huán)透明質(zhì)酸水平的升高
使用轉(zhuǎn)基因小鼠,研究人員發(fā)現(xiàn)刪除HYAL1該基因?qū)е铝烁叩钠咸烟巧桑绕涫窃谖故掣咧撅嬍车男∈笾小O喾矗词乖谝葝u素抵抗的動(dòng)物中,提高肝臟中HYAL1水平也能改善葡萄糖耐量并減少糖異生。
深入研究,該團(tuán)隊(duì)發(fā)現(xiàn)了該機(jī)制:HYAL1對(duì)HA的分解重定向了細(xì)胞尿苷二磷酸N-乙酰氨基葡萄糖(UDP-GlcNAc),減少了能量代謝關(guān)鍵線粒體蛋白質(zhì)的關(guān)鍵修飾(O-GlcNAcylation)。這會(huì)降低ATP的生成,使肝臟更難維持葡萄糖合成。重要的是,即使在胰島素抵抗的情況下,這種調(diào)節(jié)仍然有效,使其成為一個(gè)有吸引力的治療靶點(diǎn)。
雖然還需要更多的研究來量化這一途徑的作用,但這項(xiàng)研究為人體如何超越經(jīng)典胰島素精細(xì)調(diào)節(jié)葡萄糖代謝提供了新的視角-胰高血糖素系統(tǒng)。隨著糖尿病在全球范圍內(nèi)影響數(shù)百萬人,這項(xiàng)研究強(qiáng)調(diào)了代謝難題中一個(gè)被忽視但至關(guān)重要的環(huán)節(jié),這可能會(huì)導(dǎo)致新的糖尿病管理策略,如增強(qiáng)HYAL1活性或控制餐后HA水平。
參考資料
[1] Hyaluronidase-1 mediates postprandial suppression of hepatic gluconeogenesis
摘要:研究發(fā)現(xiàn),人體在進(jìn)食后調(diào)節(jié)血糖的能力方面出現(xiàn)了一個(gè)令人驚訝的新參與者
最近的一項(xiàng)研究發(fā)表于Life Metabolism發(fā)現(xiàn)了一個(gè)令人驚訝的新參與者,即身體在進(jìn)食后調(diào)節(jié)血糖的能力。
貝勒醫(yī)學(xué)院和納穆爾大學(xué)的研究人員發(fā)現(xiàn),一種名為透明質(zhì)酸酶-1(HYAL1)的酶在抑制肝臟過度葡萄糖生成方面發(fā)揮著至關(guān)重要的作用,尤其是在飯后。這一發(fā)現(xiàn)可能為治療代謝紊亂打開了新的大門,如2型糖尿病,血糖控制受損。
 圖1 透明質(zhì)酸酶-1介導(dǎo)餐后肝糖異生的抑制
圖1 透明質(zhì)酸酶-1介導(dǎo)餐后肝糖異生的抑制這項(xiàng)研究的重點(diǎn)是透明質(zhì)酸(HA),這是一種在進(jìn)食后血液中自然涌動(dòng)的糖分子。雖然HA以其在組織結(jié)構(gòu)和炎癥這項(xiàng)研究揭示了其與葡萄糖代謝的意外聯(lián)系。該團(tuán)隊(duì)發(fā)現(xiàn),HYAL1能夠分解肝臟中的HA,有助于阻止葡萄糖異生——肝臟從非碳水化合物來源產(chǎn)生葡萄糖的過程。正常情況下,餐后糖異生被抑制以防止血糖飆升,但在糖尿病患者中,糖異生仍然過度活躍。

圖2 餐后循環(huán)透明質(zhì)酸水平的升高
使用轉(zhuǎn)基因小鼠,研究人員發(fā)現(xiàn)刪除HYAL1該基因?qū)е铝烁叩钠咸烟巧桑绕涫窃谖故掣咧撅嬍车男∈笾小O喾矗词乖谝葝u素抵抗的動(dòng)物中,提高肝臟中HYAL1水平也能改善葡萄糖耐量并減少糖異生。
深入研究,該團(tuán)隊(duì)發(fā)現(xiàn)了該機(jī)制:HYAL1對(duì)HA的分解重定向了細(xì)胞尿苷二磷酸N-乙酰氨基葡萄糖(UDP-GlcNAc),減少了能量代謝關(guān)鍵線粒體蛋白質(zhì)的關(guān)鍵修飾(O-GlcNAcylation)。這會(huì)降低ATP的生成,使肝臟更難維持葡萄糖合成。重要的是,即使在胰島素抵抗的情況下,這種調(diào)節(jié)仍然有效,使其成為一個(gè)有吸引力的治療靶點(diǎn)。
雖然還需要更多的研究來量化這一途徑的作用,但這項(xiàng)研究為人體如何超越經(jīng)典胰島素精細(xì)調(diào)節(jié)葡萄糖代謝提供了新的視角-胰高血糖素系統(tǒng)。隨著糖尿病在全球范圍內(nèi)影響數(shù)百萬人,這項(xiàng)研究強(qiáng)調(diào)了代謝難題中一個(gè)被忽視但至關(guān)重要的環(huán)節(jié),這可能會(huì)導(dǎo)致新的糖尿病管理策略,如增強(qiáng)HYAL1活性或控制餐后HA水平。
參考資料
[1] Hyaluronidase-1 mediates postprandial suppression of hepatic gluconeogenesis



