摘要:研究人員揭示了遺傳因素在ICB療法耐藥性中的作用,而答案出人意料地藏在線粒體中。
黑色素瘤通常始于皮膚上一個看起來有些異常的黑斑。如果癌癥已經發展到晚期,醫生可能會建議采用免疫檢查點抑制劑來治療。這類藥物能幫助人體自身的免疫系統識別并攻擊癌細胞。
對于部分患有侵襲性黑色素瘤的患者,免疫檢查點阻斷(ICB)療法有望實現長期緩解。然而,盡管部分患者的應答狀況良好,但其他患者對ICB療法存在耐藥性。
紐約大學朗格尼醫學中心的人口健康學系副教授Tomas Kirchhoff博士表示:“由于ICB療法并非對所有人都起效,人們懷疑這可能與某種遺傳傾向有關。”
 圖1 遺傳性線粒體基因特征作為黑色素瘤免疫檢查點抑制劑療效的預測因子
圖1 遺傳性線粒體基因特征作為黑色素瘤免疫檢查點抑制劑療效的預測因子如今,Kirchhoff博士領導的研究團隊揭示了遺傳因素在這一過程中的作用,而答案出人意料地藏在線粒體中。這項研究成果于6月5日發表在《Nature Medicine》雜志上。
研究人員分析了參與CheckMate-067 III期臨床試驗的患者的血液樣本,探索了線粒體遺傳學、免疫力和治療結局之間的潛在關聯。這項臨床試驗使用了nivolumab和ipilimumab等免疫檢查點抑制劑。這些藥物通過阻斷PD-1或CTLA-4等蛋白質來發揮作用。
他們發現,線粒體DNA中攜帶特定類型遺傳突變(稱為線粒體單倍群T,HG-T)的患者對免疫檢查點療法的應答率比其他患者低3.46倍。
研究人員利用超低深度全基因組測序(lcWGS)來鑒定線粒體遺傳變異。據介紹,將lcWGS整合到更廣泛的框架中,讓他們能夠探索線粒體遺傳學如何影響免疫檢查點抑制劑的應答。
“我們從未想到線粒體遺傳學會發揮如此顯著的作用,盡管它在許多罕見疾病中很重要,” Kirchhoff談道。
這項研究表明,HG-T是患者耐受免疫檢查點抑制劑的生物標志物,獨立于其他腫瘤特征。這表明HG-T患者也許能從其他免疫檢查點抑制劑治療組合中獲益,包括近期開發的聯合療法(如阻斷其他免疫檢查點LAG-3、TIGIT和TIM-3的療法)。
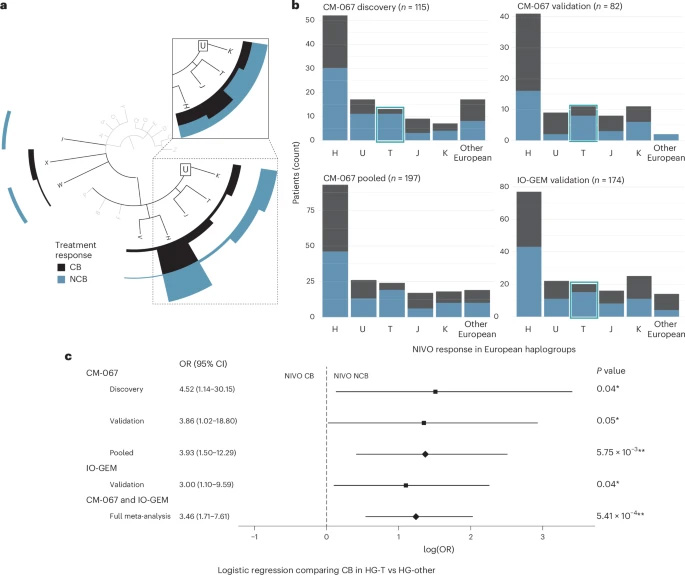
圖2 按歐洲單倍群分組的納武利尤單抗(NIVO)治療療效
盡管這項研究的重點在于宿主的免疫細胞,但研究人員強調,相同的遺傳因素也可能影響腫瘤代謝,這一領域值得深入探索并作為治療靶點。
“研究人員目前正在開展一項大型試驗,收集接受免疫檢查點抑制劑治療的其他腫瘤類型的信息,以確定這一觀察結果是否在各種癌癥中具有廣泛的臨床適用性,” Kirchhoff說。
研究還發現,特定的線粒體單倍群與血液中的免疫細胞水平降低相關。具體來說,與非HG-T患者相比,對治療耐藥的HG-T患者具有更多發育不全的T細胞。他們將這種分化不良歸因于對活性氧(ROS)的恢復力增加。
研究人員表示,這項研究首次揭示了線粒體遺傳、宿主免疫和免疫檢查點抑制劑耐藥性之間的關聯。它提出了一種基于宿主血液的生物標志物,具有獨立的臨床價值,可以預測免疫檢查點抑制劑的療效。
下一步,研究人員希望開發出一種臨床檢測方法,以確定那些可能無法從免疫檢查點抑制劑治療中獲益的患者,避免讓患者接受可能具有毒性且無效的治療。
參考資料
[1] Inherited mitochondrial genetics as a predictor of immune checkpoint inhibition efficacy in melanoma
摘要:研究人員揭示了遺傳因素在ICB療法耐藥性中的作用,而答案出人意料地藏在線粒體中。
黑色素瘤通常始于皮膚上一個看起來有些異常的黑斑。如果癌癥已經發展到晚期,醫生可能會建議采用免疫檢查點抑制劑來治療。這類藥物能幫助人體自身的免疫系統識別并攻擊癌細胞。
對于部分患有侵襲性黑色素瘤的患者,免疫檢查點阻斷(ICB)療法有望實現長期緩解。然而,盡管部分患者的應答狀況良好,但其他患者對ICB療法存在耐藥性。
紐約大學朗格尼醫學中心的人口健康學系副教授Tomas Kirchhoff博士表示:“由于ICB療法并非對所有人都起效,人們懷疑這可能與某種遺傳傾向有關。”
 圖1 遺傳性線粒體基因特征作為黑色素瘤免疫檢查點抑制劑療效的預測因子
圖1 遺傳性線粒體基因特征作為黑色素瘤免疫檢查點抑制劑療效的預測因子如今,Kirchhoff博士領導的研究團隊揭示了遺傳因素在這一過程中的作用,而答案出人意料地藏在線粒體中。這項研究成果于6月5日發表在《Nature Medicine》雜志上。
研究人員分析了參與CheckMate-067 III期臨床試驗的患者的血液樣本,探索了線粒體遺傳學、免疫力和治療結局之間的潛在關聯。這項臨床試驗使用了nivolumab和ipilimumab等免疫檢查點抑制劑。這些藥物通過阻斷PD-1或CTLA-4等蛋白質來發揮作用。
他們發現,線粒體DNA中攜帶特定類型遺傳突變(稱為線粒體單倍群T,HG-T)的患者對免疫檢查點療法的應答率比其他患者低3.46倍。
研究人員利用超低深度全基因組測序(lcWGS)來鑒定線粒體遺傳變異。據介紹,將lcWGS整合到更廣泛的框架中,讓他們能夠探索線粒體遺傳學如何影響免疫檢查點抑制劑的應答。
“我們從未想到線粒體遺傳學會發揮如此顯著的作用,盡管它在許多罕見疾病中很重要,” Kirchhoff談道。
這項研究表明,HG-T是患者耐受免疫檢查點抑制劑的生物標志物,獨立于其他腫瘤特征。這表明HG-T患者也許能從其他免疫檢查點抑制劑治療組合中獲益,包括近期開發的聯合療法(如阻斷其他免疫檢查點LAG-3、TIGIT和TIM-3的療法)。

圖2 按歐洲單倍群分組的納武利尤單抗(NIVO)治療療效
盡管這項研究的重點在于宿主的免疫細胞,但研究人員強調,相同的遺傳因素也可能影響腫瘤代謝,這一領域值得深入探索并作為治療靶點。
“研究人員目前正在開展一項大型試驗,收集接受免疫檢查點抑制劑治療的其他腫瘤類型的信息,以確定這一觀察結果是否在各種癌癥中具有廣泛的臨床適用性,” Kirchhoff說。
研究還發現,特定的線粒體單倍群與血液中的免疫細胞水平降低相關。具體來說,與非HG-T患者相比,對治療耐藥的HG-T患者具有更多發育不全的T細胞。他們將這種分化不良歸因于對活性氧(ROS)的恢復力增加。
研究人員表示,這項研究首次揭示了線粒體遺傳、宿主免疫和免疫檢查點抑制劑耐藥性之間的關聯。它提出了一種基于宿主血液的生物標志物,具有獨立的臨床價值,可以預測免疫檢查點抑制劑的療效。
下一步,研究人員希望開發出一種臨床檢測方法,以確定那些可能無法從免疫檢查點抑制劑治療中獲益的患者,避免讓患者接受可能具有毒性且無效的治療。
參考資料
[1] Inherited mitochondrial genetics as a predictor of immune checkpoint inhibition efficacy in melanoma



