隨著對RNA研究的不斷深入,人們發現,非編碼RNA的突變或表達異常與許多疾病的發生密切相關。ncRNA 可以按照不同長度上來劃分,例如長度大于200nt的ncRNA被稱為長鏈非編碼RNA(lncRNA),而長度低于50nt的則被稱為 small RNA,包括我們熟悉的miRNA。
此外,ncRNA還可以根據形態結構區分為線性和非線性,環狀RNA(circRNA)即是一類分子呈封閉環狀結構的特殊類型ncRNA。細胞中含量很高的ncRNA是rRNA 和tRNA ,研究相對透徹。近年來有關lncRNA、miRNA和circRNA在細胞中的生理、病理作用機制及其之間的調控網絡得到越來越多的關注。
以往的研究證實,circRNA能作為miRNA海綿(sponge),解除miRNA對靶基因的抑制作用,從而調控基因表達,并在腫瘤的發生發展中發揮重要作用。非編碼RNA不僅不是“垃圾RNA”,還有可能調動其它的類型的非編碼RNA,發揮重要作用!

2022年1月4日,來自香港中文大學醫學院、中山大學附屬第七醫院的研究團隊在Molecular Cancer在線發表了題為“CircRTN4promotes pancreatic cancer progression through a novel CircRNA-miRNA-lncRNApathway and stabilizing epithelial-mesenchymal transition protein”的文章。研究人員在胰島管腺癌(PDAC)中發現了一個新的促癌的circRNA- miRNA – lncRNA信號通路,且這3個分子均是非編碼RNA。除了調節lncRNA的表達外,研究還發現circRTN4能與上皮間質轉化(epithelial-mesenchymaltransition, EMT)驅動蛋白RAB11FIP1相互作用,增強其穩定性并促進EMT發生。研究結果拓寬了對circRNA在PDAC基因表達調控中的作用的認識。
在前期工作的基礎上,研究人員重點關注一種名為circRTN4的環狀RNA。細胞水平的檢測顯示,circRTN4在幾種不同類型的PDAC細胞系中均顯著上調。在88例PDAC患者中,circRTN4上調的患者比例高達60%。此外,在結直腸癌、喉部鱗狀細胞癌、頭頸部鱗狀細胞癌、卵巢癌、腎癌等多種腫瘤中也出現類似的結果。研究團隊分析了circRTN4的表達水平與臨床特征之間的相關性,發現肝轉移的PDAC患者原發腫瘤中circRTN4表達水平顯著上調,提示PDAC原發腫瘤中circRTN4表達上調可能參與了腫瘤肝轉移。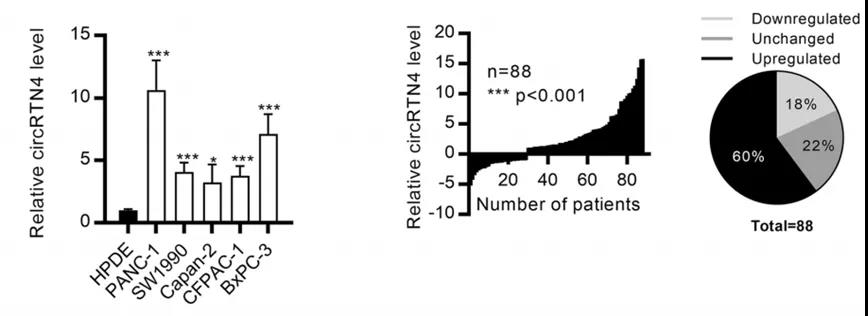
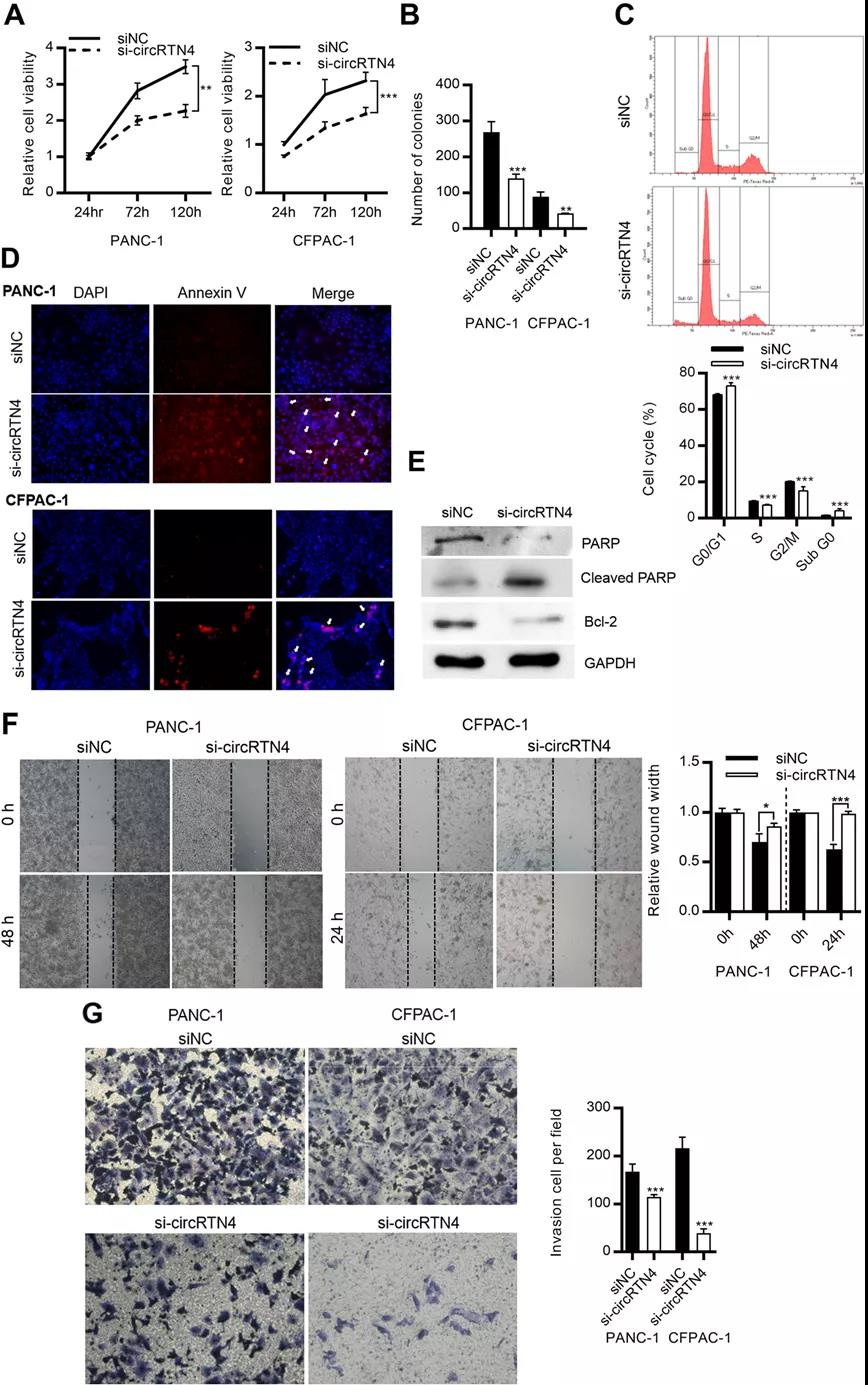

為驗證這種相關性是否具有因果關聯,研究人員進行了細胞水平的circRNA敲降實驗,發現敲降circRNA后,PDAC細胞系的增殖、克隆形成、遷移和侵襲能力均較對照組明顯減弱。

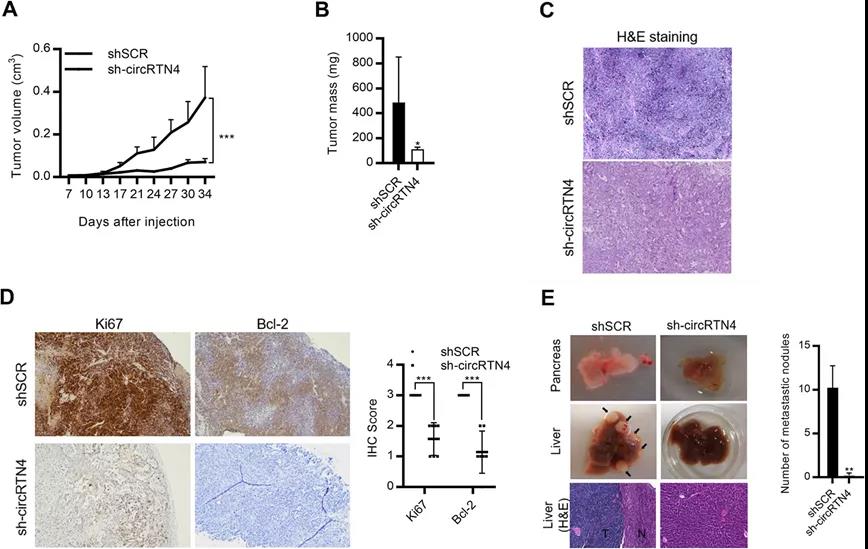
基于小鼠移植瘤模型體內實驗進一步證實了抑制circRNA后,腫瘤的生長放緩,凋亡增加,肝轉移減少。

體內、體外實驗結果充分說明了circRTN4在促進PDAC細胞生長和侵襲中的重要性。接下來,研究人員試圖尋找該分子發揮作用的具體分子機制。借助生物信息學預測軟件,研究人員篩選了可能與circRTN4結合的miRNA,隨后通過熒光素酶報告分析、miRNA pull down、生物素標記等多種實驗手段證實了PDAC細胞circRTN4與miR-497-5p存在相互作用,并且circRNA通過經典的“sponge”(吸附)效應,抑制miR-497-5p的功能。
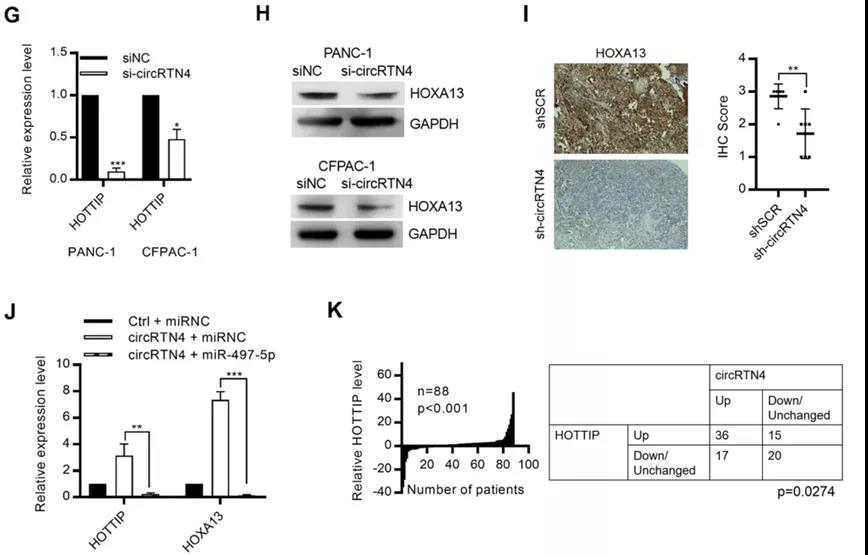
此前已有多個文獻報道miR-497-5p通過靶向致癌HOTTIP-HOXA13通路( HOTTIP是來源于HOXA的5′端的一個長鏈非編碼RNA。HOTTIP-HOXA13與疾病發生的關系非常密切)在PDAC中發揮抑癌作用。
那么,circRTN4會否通過“sponge”效應抑制PDAC中的miR-497-5p,從而調控HOTTIP-HOXA13通路?相關的實驗數據顯示,circRTN4的確通過抑制miR-497-5p,影響了lncRNA HOTTIP的表達,首次在PDAC中發現了由3個不同類型的非編碼RNA組成的circRTN4-miR-497-5p-lncRNAHOTTIP這一信號軸。

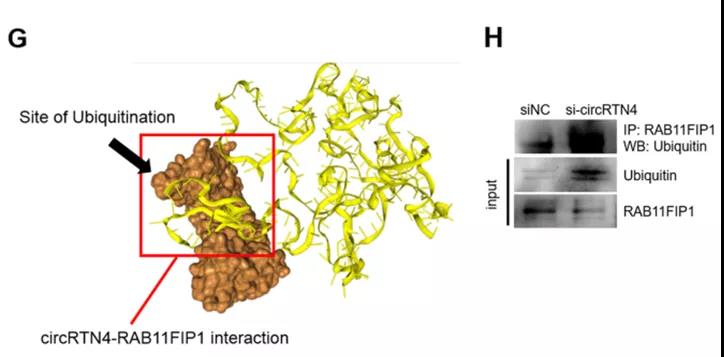
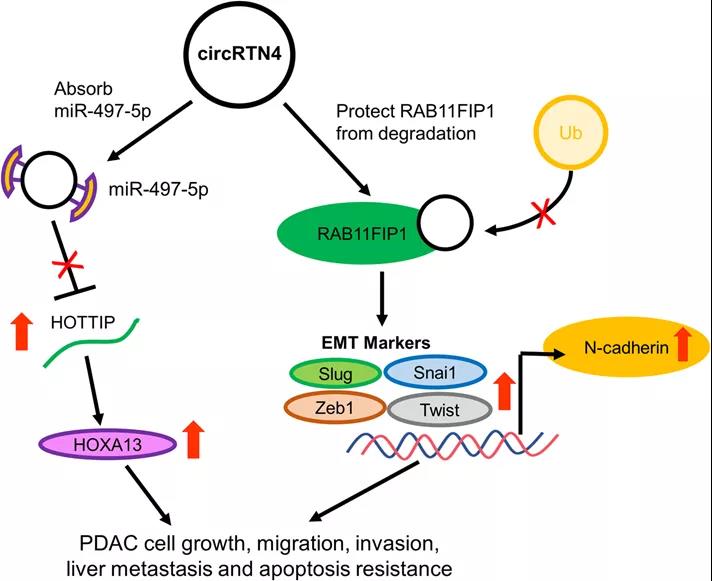
盡管circRNA-miRNA這種相互作用模式是circRNA在PDAC中報道較多的模式,但許多細胞系中circRNA的豐度都比miRNA低得多,表明circRNA在PDAC中可能有其他獨立于miRNA的作用機制。為解決這個問題,研究人員circRTN4尋找與之相互作用的蛋白質,識別出了EMT驅動因子RAB11FIP1以及其與cirRTN4的結合位點。一系列實驗結果顯示,cirRTN4通過阻斷RAB11FIP1的泛素化來穩定RAB11FIP1,促進N-cadherin、Slug、Snai1、Twist和Zeb1等EMT通路關鍵分子的表達,并促進PDAC的EMT。

總之,該研究揭示了一種新的促進PDAC進展的circRNA-miRNA-lncRNA途徑以及circRTN4通過阻斷泛素化促進EMT的機制,為circRTN4的促癌能力提供了新的視角。circRTN4或許能成為一種新的生物標志物和PDAC潛在治療靶點。




