睡眠時(shí)間是衡量人體健康狀況的重要指標(biāo),肝臟是維持生命所必需的,在新陳代謝中起著重要作用。非酒精性脂肪性肝病(Non-alcoholic Fatty Liver Disease,NAFLD)是一種由脂肪過(guò)度堆積引起的代謝性肝病,全球發(fā)病率很高。NAFLD包括一系列的肝臟損害,從單純性脂肪變性到非酒精性脂肪性肝炎,如果不加以預(yù)防,可能會(huì)導(dǎo)致肝硬化和肝癌。

睡眠不足和睡眠質(zhì)量差會(huì)引發(fā)多個(gè)與NAFLD相關(guān)的病理生理過(guò)程
既往研究發(fā)現(xiàn),睡眠不足與肝纖維化呈負(fù)相關(guān),睡眠不足和睡眠質(zhì)量差會(huì)引發(fā)多個(gè)與NAFLD相關(guān)的病理生理過(guò)程。近日,發(fā)表在Hepatology雜志的一篇題為“Weekend catch-up sleep is associated with the alleviation of non-alcoholic fatty liver disease”的研究顯示:周末補(bǔ)覺(jué)可緩解非酒精性脂肪肝(圖1)。
 研究顯示:周末補(bǔ)覺(jué)可緩解非酒精性脂肪肝
研究顯示:周末補(bǔ)覺(jué)可緩解非酒精性脂肪肝圖1 研究成果(圖源:[1])
本研究記錄2008-2019年來(lái)自韓國(guó)國(guó)民健康和營(yíng)養(yǎng)調(diào)查(Korea National Health and Nutrition Examination Survey,KNHANES)中有關(guān)睡眠時(shí)間的數(shù)據(jù)。由于KNHANES在2016年收集的睡眠時(shí)長(zhǎng)不同,根據(jù)收集的睡眠時(shí)長(zhǎng)類型將總數(shù)據(jù)分為集合1(n=26988)和集合2(n=11714)。根據(jù)睡眠持續(xù)時(shí)間不同將受試者分為3組:第1組,平均每日睡眠小于7小時(shí);第2組,平均工作日睡眠不足7小時(shí),周末平均睡眠超過(guò)7小時(shí)(WCUS模式);第3組:平均每日睡眠時(shí)間大于或等于7小時(shí)。然后,采用多因素Logistic回歸分析每組睡眠時(shí)間與NAFLD的相關(guān)性。
本研究中使用肝臟脂肪變性指數(shù)(hepatic steatosis index,HSI)來(lái)確定脂肪肝的存在。HSI計(jì)算公式為:HSI=8×(ALT/AST)+BMI(女性+2,糖尿病+2),HSI≥36被認(rèn)為是脂肪肝的指標(biāo)(ALT:alanine aminotransferase,谷丙轉(zhuǎn)氨酶;AST:aspartate aminotransferase,谷草轉(zhuǎn)氨酶;BMI:body mass index,體重指數(shù))。以平均每日睡眠時(shí)間<7小時(shí)為基準(zhǔn),從KNHANES(2008-2015年)的數(shù)據(jù)分析顯示,平均每日睡眠時(shí)間≥7h與患NAFLD風(fēng)險(xiǎn)呈顯著負(fù)相關(guān)。即使使用KNHANES(2016-2019年)的數(shù)據(jù)將睡眠時(shí)間劃分為工作日和周末進(jìn)行分析,睡眠時(shí)間≥7h也顯示出與患NAFLD風(fēng)險(xiǎn)呈顯著負(fù)相關(guān)。此外,當(dāng)將受試者分為男性和女性進(jìn)行分析時(shí),結(jié)果相似(表1)。
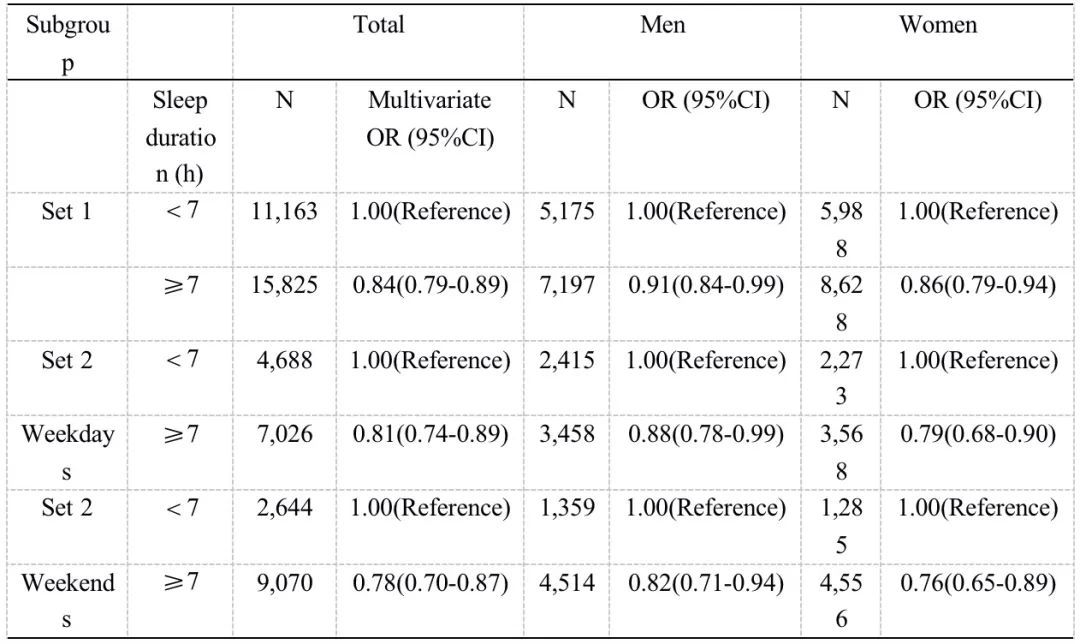 表1 臨床相關(guān)亞組中睡眠時(shí)間和質(zhì)量與NAFLD風(fēng)險(xiǎn)的關(guān)系
表1 臨床相關(guān)亞組中睡眠時(shí)間和質(zhì)量與NAFLD風(fēng)險(xiǎn)的關(guān)系表格來(lái)源:[1]
在KNHANES數(shù)據(jù)集合2中,第1、2、3組分別納入了2365(20.2%)、2602(22.2%)和6747(57.6%)名受試者。以第1組為基準(zhǔn),第2、3組患NAFLD的風(fēng)險(xiǎn)都減低;而將受試者分為男性組和女性組進(jìn)行對(duì)照分析時(shí),發(fā)現(xiàn)第2、3組患NAFLD的風(fēng)險(xiǎn)也都減低。此外,在對(duì)肥胖和代謝綜合征受試者的分析中發(fā)現(xiàn),以第1組為基準(zhǔn),第2、3組患NAFLD的風(fēng)險(xiǎn)減低。本研究還對(duì)WCUS與ALT異常及肥胖的關(guān)系進(jìn)行了分析,以第1組為基準(zhǔn),當(dāng)ALT≥40IU/L或BMI≥25 kg/m2時(shí),第2組和第3組患NAFLD的風(fēng)險(xiǎn)都減低。總之,該研究顯示,睡眠充足和WCUS的人患NAFLD的風(fēng)險(xiǎn)比睡眠不足的人低。
NAFLD在我國(guó)的治療進(jìn)展
近年來(lái),脂肪性肝病現(xiàn)已取代慢性乙型肝炎成為我國(guó)較常見(jiàn)的慢性肝病。在我國(guó)NAFLD患者人數(shù)迅速增加,且發(fā)病年齡呈低齡化趨勢(shì),已逐步成為重要的公共健康問(wèn)題,NAFLD的預(yù)防和治療也逐漸成為代謝疾病領(lǐng)域的研究熱點(diǎn)之一。那目前NAFLD主流治療方法有哪些呢?
1、生活行為糾正
目前普遍被接受的減重是非酒精性脂肪性肝炎(Non-alcoholic Steatohepatitis,NASH)病人肝臟組織學(xué)特性改善的較強(qiáng)相關(guān)因素,日常生活行為的糾正,包括健康飲食(拒絕高卡路里、高脂和高糖飲食)、拒絕酒精和加強(qiáng)體育鍛煉,已經(jīng)成為NAFLD和NASH的一線治療策略。
2、藥物治療
據(jù)統(tǒng)計(jì),截至2020年底,全球共計(jì)約有175種相關(guān)藥物在研,其中35種目前處于臨床Ⅰ期研究中,78種處于臨床Ⅱ期或Ⅲ期研究中。雖然申報(bào)數(shù)量龐大,但結(jié)果卻不盡如人意,至今全球尚無(wú)獲批用于治療NAFLD的藥物。若非必須,任何具體藥物療法都不應(yīng)被臨床醫(yī)生推薦。但使用吡格列酮、維生素E(800 U/d)可改善NASH患者的肝組織學(xué)特征。因此在與病人溝通治療方案的風(fēng)險(xiǎn)之后,可考慮將上述兩種藥物用于NASH病人(吡格列酮可能引起噻唑烷二酮類藥物常見(jiàn)的不良反應(yīng):高危人群的體重增加、足部水腫、骨質(zhì)流失和充血性心力衰竭,而飲食中補(bǔ)充維生素E則可能顯著增加健康男性罹患前列腺癌的風(fēng)險(xiǎn))。
3、外科治療
對(duì)于行為糾正以及藥物治療不敏感的NASH病人,減重手術(shù)或許是有效的替代方案。減重手術(shù)是近年來(lái)快速發(fā)展的一種有效的減重療法。而不論減重手術(shù)抑或行為糾正所導(dǎo)致的有效減重,都被證實(shí)能夠顯著改善NASH病人的肝組織學(xué)特性。
NASH潛在治療新靶點(diǎn)在國(guó)內(nèi)獲得突破
2022年3月12日,南京醫(yī)科大學(xué)呂凌團(tuán)隊(duì)在期刊Journal of Hepatology上發(fā)表了一篇題為“Role of XBP1 in regulating the progression of non-alcoholic steatohepatitis”的研究論著,發(fā)現(xiàn)了XBP1抑制劑可作為NASH的潛在治療新靶點(diǎn)(圖2)。
 XBP1抑制劑可作為NASH的潛在治療新靶點(diǎn)
XBP1抑制劑可作為NASH的潛在治療新靶點(diǎn)圖2 研究成果(圖源:[2])
該研究從NASH患者和對(duì)照組獲得人肝組織用于評(píng)估X-box結(jié)合蛋白-1(XBP1)的表達(dá),NASH模型是在肝細(xì)胞特異性Xbp1敲除 (Xbp1ΔHep)、巨噬細(xì)胞特異性Xbp1敲除 (Xbp1ΔM?)、巨噬細(xì)胞特異性Nlrp3敲除和野生型(Xbp1FL/FL或Nlrp3FL/FL)小鼠喂食高脂飲食26周或蛋氨酸/膽堿缺乏飲食6周。該研究結(jié)果顯示XBP1的表達(dá)在NASH患者的肝臟樣本中顯著上調(diào),可調(diào)節(jié)NASH的發(fā)展,XBP1抑制劑可預(yù)防脂肪性肝炎,從而可作為治療NASH的潛在靶點(diǎn)。
熬夜的壞處人盡皆知,但在如今快節(jié)奏的生活中,很少有人能做到不熬夜,通過(guò)周末補(bǔ)覺(jué)緩解平時(shí)熬夜帶來(lái)的危害也不失為一種解決辦法。基于這項(xiàng)研究,我們了解了周末補(bǔ)覺(jué)對(duì)于緩解非酒精性脂肪肝的重要意義。因此,除了生活行為糾正、藥物治療和外科治療外,針對(duì)NAFLD的治療方法將不斷取得新進(jìn)展,為廣大NAFLD患者帶來(lái)新希望。
參考資料:
[1]Seo Y, Sung GH, Lee S, et al. Weekend catch-up sleep is associated with the alleviation of non-alcoholic fatty liver disease. Ann Hepatol. 2022 Feb 20:100690. doi: 10.1016/j.aohep.2022.100690. Epub ahead of print. PMID: 35196551.
[2]Qi Wang, Haoming Zhou, Qingfa Bu, et al. Role of XBP1 in regulating the progression of non-alcoholic steatohepatitis. Journal of Hepatology. 2022 Mar 12. doi: https://doi.org/10.1016/j.jhep.2022.02.031.
睡眠時(shí)間是衡量人體健康狀況的重要指標(biāo),肝臟是維持生命所必需的,在新陳代謝中起著重要作用。非酒精性脂肪性肝病(Non-alcoholic Fatty Liver Disease,NAFLD)是一種由脂肪過(guò)度堆積引起的代謝性肝病,全球發(fā)病率很高。NAFLD包括一系列的肝臟損害,從單純性脂肪變性到非酒精性脂肪性肝炎,如果不加以預(yù)防,可能會(huì)導(dǎo)致肝硬化和肝癌。

睡眠不足和睡眠質(zhì)量差會(huì)引發(fā)多個(gè)與NAFLD相關(guān)的病理生理過(guò)程
既往研究發(fā)現(xiàn),睡眠不足與肝纖維化呈負(fù)相關(guān),睡眠不足和睡眠質(zhì)量差會(huì)引發(fā)多個(gè)與NAFLD相關(guān)的病理生理過(guò)程。近日,發(fā)表在Hepatology雜志的一篇題為“Weekend catch-up sleep is associated with the alleviation of non-alcoholic fatty liver disease”的研究顯示:周末補(bǔ)覺(jué)可緩解非酒精性脂肪肝(圖1)。
 研究顯示:周末補(bǔ)覺(jué)可緩解非酒精性脂肪肝
研究顯示:周末補(bǔ)覺(jué)可緩解非酒精性脂肪肝圖1 研究成果(圖源:[1])
本研究記錄2008-2019年來(lái)自韓國(guó)國(guó)民健康和營(yíng)養(yǎng)調(diào)查(Korea National Health and Nutrition Examination Survey,KNHANES)中有關(guān)睡眠時(shí)間的數(shù)據(jù)。由于KNHANES在2016年收集的睡眠時(shí)長(zhǎng)不同,根據(jù)收集的睡眠時(shí)長(zhǎng)類型將總數(shù)據(jù)分為集合1(n=26988)和集合2(n=11714)。根據(jù)睡眠持續(xù)時(shí)間不同將受試者分為3組:第1組,平均每日睡眠小于7小時(shí);第2組,平均工作日睡眠不足7小時(shí),周末平均睡眠超過(guò)7小時(shí)(WCUS模式);第3組:平均每日睡眠時(shí)間大于或等于7小時(shí)。然后,采用多因素Logistic回歸分析每組睡眠時(shí)間與NAFLD的相關(guān)性。
本研究中使用肝臟脂肪變性指數(shù)(hepatic steatosis index,HSI)來(lái)確定脂肪肝的存在。HSI計(jì)算公式為:HSI=8×(ALT/AST)+BMI(女性+2,糖尿病+2),HSI≥36被認(rèn)為是脂肪肝的指標(biāo)(ALT:alanine aminotransferase,谷丙轉(zhuǎn)氨酶;AST:aspartate aminotransferase,谷草轉(zhuǎn)氨酶;BMI:body mass index,體重指數(shù))。以平均每日睡眠時(shí)間<7小時(shí)為基準(zhǔn),從KNHANES(2008-2015年)的數(shù)據(jù)分析顯示,平均每日睡眠時(shí)間≥7h與患NAFLD風(fēng)險(xiǎn)呈顯著負(fù)相關(guān)。即使使用KNHANES(2016-2019年)的數(shù)據(jù)將睡眠時(shí)間劃分為工作日和周末進(jìn)行分析,睡眠時(shí)間≥7h也顯示出與患NAFLD風(fēng)險(xiǎn)呈顯著負(fù)相關(guān)。此外,當(dāng)將受試者分為男性和女性進(jìn)行分析時(shí),結(jié)果相似(表1)。

表1 臨床相關(guān)亞組中睡眠時(shí)間和質(zhì)量與NAFLD風(fēng)險(xiǎn)的關(guān)系
表格來(lái)源:[1]
在KNHANES數(shù)據(jù)集合2中,第1、2、3組分別納入了2365(20.2%)、2602(22.2%)和6747(57.6%)名受試者。以第1組為基準(zhǔn),第2、3組患NAFLD的風(fēng)險(xiǎn)都減低;而將受試者分為男性組和女性組進(jìn)行對(duì)照分析時(shí),發(fā)現(xiàn)第2、3組患NAFLD的風(fēng)險(xiǎn)也都減低。此外,在對(duì)肥胖和代謝綜合征受試者的分析中發(fā)現(xiàn),以第1組為基準(zhǔn),第2、3組患NAFLD的風(fēng)險(xiǎn)減低。本研究還對(duì)WCUS與ALT異常及肥胖的關(guān)系進(jìn)行了分析,以第1組為基準(zhǔn),當(dāng)ALT≥40IU/L或BMI≥25 kg/m2時(shí),第2組和第3組患NAFLD的風(fēng)險(xiǎn)都減低。總之,該研究顯示,睡眠充足和WCUS的人患NAFLD的風(fēng)險(xiǎn)比睡眠不足的人低。
NAFLD在我國(guó)的治療進(jìn)展
近年來(lái),脂肪性肝病現(xiàn)已取代慢性乙型肝炎成為我國(guó)較常見(jiàn)的慢性肝病。在我國(guó)NAFLD患者人數(shù)迅速增加,且發(fā)病年齡呈低齡化趨勢(shì),已逐步成為重要的公共健康問(wèn)題,NAFLD的預(yù)防和治療也逐漸成為代謝疾病領(lǐng)域的研究熱點(diǎn)之一。那目前NAFLD主流治療方法有哪些呢?
1、生活行為糾正
目前普遍被接受的減重是非酒精性脂肪性肝炎(Non-alcoholic Steatohepatitis,NASH)病人肝臟組織學(xué)特性改善的較強(qiáng)相關(guān)因素,日常生活行為的糾正,包括健康飲食(拒絕高卡路里、高脂和高糖飲食)、拒絕酒精和加強(qiáng)體育鍛煉,已經(jīng)成為NAFLD和NASH的一線治療策略。
2、藥物治療
據(jù)統(tǒng)計(jì),截至2020年底,全球共計(jì)約有175種相關(guān)藥物在研,其中35種目前處于臨床Ⅰ期研究中,78種處于臨床Ⅱ期或Ⅲ期研究中。雖然申報(bào)數(shù)量龐大,但結(jié)果卻不盡如人意,至今全球尚無(wú)獲批用于治療NAFLD的藥物。若非必須,任何具體藥物療法都不應(yīng)被臨床醫(yī)生推薦。但使用吡格列酮、維生素E(800 U/d)可改善NASH患者的肝組織學(xué)特征。因此在與病人溝通治療方案的風(fēng)險(xiǎn)之后,可考慮將上述兩種藥物用于NASH病人(吡格列酮可能引起噻唑烷二酮類藥物常見(jiàn)的不良反應(yīng):高危人群的體重增加、足部水腫、骨質(zhì)流失和充血性心力衰竭,而飲食中補(bǔ)充維生素E則可能顯著增加健康男性罹患前列腺癌的風(fēng)險(xiǎn))。
3、外科治療
對(duì)于行為糾正以及藥物治療不敏感的NASH病人,減重手術(shù)或許是有效的替代方案。減重手術(shù)是近年來(lái)快速發(fā)展的一種有效的減重療法。而不論減重手術(shù)抑或行為糾正所導(dǎo)致的有效減重,都被證實(shí)能夠顯著改善NASH病人的肝組織學(xué)特性。
NASH潛在治療新靶點(diǎn)在國(guó)內(nèi)獲得突破
2022年3月12日,南京醫(yī)科大學(xué)呂凌團(tuán)隊(duì)在期刊Journal of Hepatology上發(fā)表了一篇題為“Role of XBP1 in regulating the progression of non-alcoholic steatohepatitis”的研究論著,發(fā)現(xiàn)了XBP1抑制劑可作為NASH的潛在治療新靶點(diǎn)(圖2)。
 XBP1抑制劑可作為NASH的潛在治療新靶點(diǎn)
XBP1抑制劑可作為NASH的潛在治療新靶點(diǎn)圖2 研究成果(圖源:[2])
該研究從NASH患者和對(duì)照組獲得人肝組織用于評(píng)估X-box結(jié)合蛋白-1(XBP1)的表達(dá),NASH模型是在肝細(xì)胞特異性Xbp1敲除 (Xbp1ΔHep)、巨噬細(xì)胞特異性Xbp1敲除 (Xbp1ΔM?)、巨噬細(xì)胞特異性Nlrp3敲除和野生型(Xbp1FL/FL或Nlrp3FL/FL)小鼠喂食高脂飲食26周或蛋氨酸/膽堿缺乏飲食6周。該研究結(jié)果顯示XBP1的表達(dá)在NASH患者的肝臟樣本中顯著上調(diào),可調(diào)節(jié)NASH的發(fā)展,XBP1抑制劑可預(yù)防脂肪性肝炎,從而可作為治療NASH的潛在靶點(diǎn)。
熬夜的壞處人盡皆知,但在如今快節(jié)奏的生活中,很少有人能做到不熬夜,通過(guò)周末補(bǔ)覺(jué)緩解平時(shí)熬夜帶來(lái)的危害也不失為一種解決辦法。基于這項(xiàng)研究,我們了解了周末補(bǔ)覺(jué)對(duì)于緩解非酒精性脂肪肝的重要意義。因此,除了生活行為糾正、藥物治療和外科治療外,針對(duì)NAFLD的治療方法將不斷取得新進(jìn)展,為廣大NAFLD患者帶來(lái)新希望。
參考資料:
[1]Seo Y, Sung GH, Lee S, et al. Weekend catch-up sleep is associated with the alleviation of non-alcoholic fatty liver disease. Ann Hepatol. 2022 Feb 20:100690. doi: 10.1016/j.aohep.2022.100690. Epub ahead of print. PMID: 35196551.
[2]Qi Wang, Haoming Zhou, Qingfa Bu, et al. Role of XBP1 in regulating the progression of non-alcoholic steatohepatitis. Journal of Hepatology. 2022 Mar 12. doi: https://doi.org/10.1016/j.jhep.2022.02.031.



