摘要:馬里蘭大學醫學院(UMSOM)精確疾病建模中心的研究人員確定了導致COVID-19的SARS-CoV-2病毒中的一種特定蛋白質是如何損害心臟組織的。然后他們使用一種藥物來逆轉這種蛋白質對心臟的毒性作用。
馬里蘭大學醫學院(UMSOM)精確疾病建模中心的研究人員確定了導致COVID-19的SARS-CoV-2病毒中的一種特定蛋白質是如何損害心臟組織的。然后他們使用一種藥物來逆轉這種蛋白質對心臟的毒性作用。
他們的發現是基于對果蠅和小鼠心臟細胞的研究,發表于2022年9月30日的Communications Biology。

圖1 研究人員確定了SARS-CoV-2病毒中的特定蛋白質如何損害心臟組織(圖源:[1])
與未感染病毒的人相比,感染COVID-19的人在感染后至少一年內發生心肌炎癥、心律異常、血凝塊、中風、心臟病發作和心力衰竭的風險明顯更高。盡管科學家們迅速開發出疫苗和藥物來減輕COVID-19疾病的嚴重程度,但這些療法并不能保護心臟或其他器官免受即使是輕微感染也可能造成的損害。
“要長期治療患者,我們必須首先了解導致疾病的機制。我們的研究表明,單個的SARS-CoV-2蛋白質都可以對身體的特定組織造成重大損害,這與對其他病毒如艾滋病毒和寨卡病毒的發現類似,”高級作者、醫學教授、密歇根大學醫學院精確疾病建模中心主任Zhe Han博士說。“通過識別每個組織中的這些損傷過程,我們可以測試藥物,看看是否有任何藥物可以逆轉這種損傷;那些表現出希望的藥物可以在臨床研究研究中進一步測試。”
去年,Han博士和他的研究團隊在使用果蠅和人類細胞的研究中發現了毒性最強的SARS-CoV-2蛋白。他們發現了一種很有前途的藥物selinexor降低了其中一種蛋白質的毒性,但沒有降低另一種被稱為Nsp6的蛋白質的毒性。
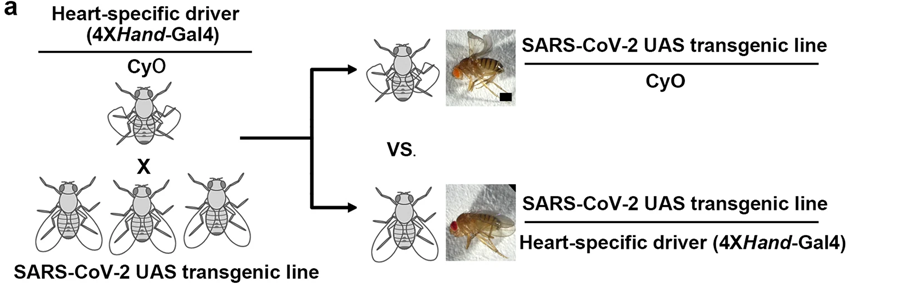
圖2 遺傳篩選示意圖,通過心臟病理學識別特定的SARS-CoV-2基因(圖源:[1])
在他們最新的研究中,他們發現Nsp6是果蠅心臟中毒性最大的SARS-CoV-2蛋白。接下來,他們發現Nsp6蛋白質劫持了果蠅心臟中的細胞,啟動糖酵解過程,使細胞燃燒葡萄糖為能量。通常情況下,心臟細胞使用脂肪酸作為能量來源,但在心力衰竭時,這些細胞會轉換到糖代謝,試圖修復受損組織。研究人員還發現,Nsp6蛋白破壞了細胞的動力源——線粒體,線粒體通過糖代謝產生能量,從而增加了損傷。
然后,研究小組使用2-脫氧葡萄糖(2DG)阻斷果蠅和小鼠心臟細胞的糖代謝。他們發現這種藥物減少了由Nsp6病毒蛋白引起的心臟和線粒體損傷。
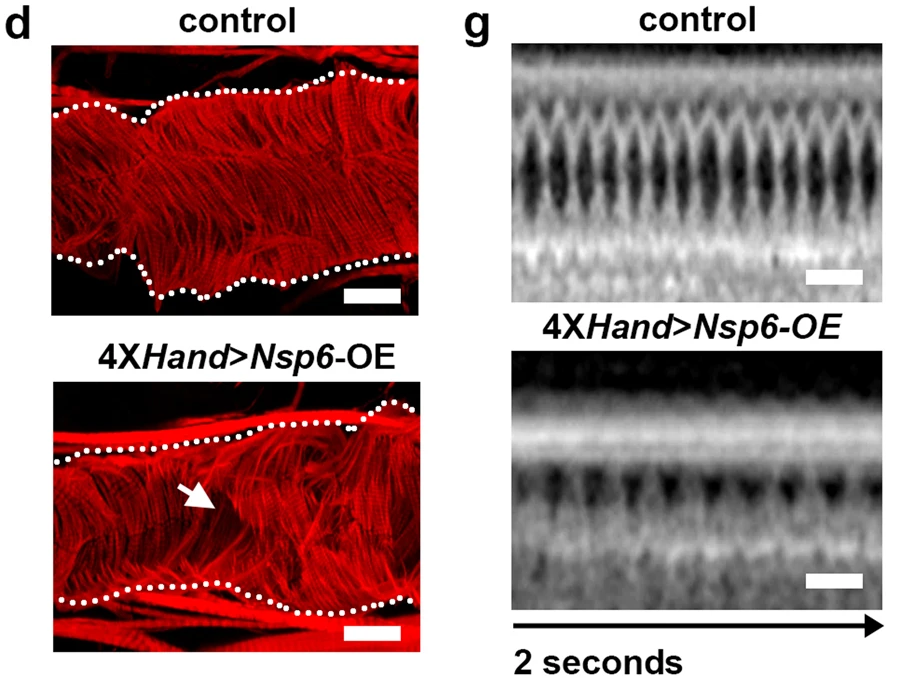
圖3 UAS-SARS-CoV-2Nsp6轉基因的4XH和Gal4、成纖維細胞特異性過表達(OE)誘導的成人心臟表型(圖源:[1])
“我們知道,一些病毒劫持受感染動物的細胞機制,改變其新陳代謝,竊取細胞的能量來源,所以我們懷疑SARS-CoV-2做了類似的事情。病毒還可以利用糖代謝的副產品作為制造更多病毒的基石,”Han博士說。“因此,我們預測這種將心臟新陳代謝改變到感染前的藥物對病毒是有害的,因為它既切斷了病毒的能量供應,也消除了病毒復制所需的片段。”
研究人員說,幸運的是,2DG很便宜,在實驗室研究中經常使用。盡管2DG尚未獲得美國食品和藥物管理局的批準用于治療疾病,但該藥物目前正在印度進行治療COVID-19的臨床試驗。
很多從COVID康復的美國人在幾周或幾個月后出現了危險的心臟疾病,我們需要了解發生這種情況的根本原因。隨著這項研究闡明了Nsp6蛋白的途徑,我們可以為未來的研究改進我們的治療目標,最終目標是逆轉這些患者的進一步心臟損傷。
參考資料:
[1] SARS-CoV-2 Nsp6 damages Drosophila heart and mouse cardiomyocytes through MGA/MAX complex-mediated increased glycolysis
摘要:馬里蘭大學醫學院(UMSOM)精確疾病建模中心的研究人員確定了導致COVID-19的SARS-CoV-2病毒中的一種特定蛋白質是如何損害心臟組織的。然后他們使用一種藥物來逆轉這種蛋白質對心臟的毒性作用。
馬里蘭大學醫學院(UMSOM)精確疾病建模中心的研究人員確定了導致COVID-19的SARS-CoV-2病毒中的一種特定蛋白質是如何損害心臟組織的。然后他們使用一種藥物來逆轉這種蛋白質對心臟的毒性作用。
他們的發現是基于對果蠅和小鼠心臟細胞的研究,發表于2022年9月30日的Communications Biology。

圖1 研究人員確定了SARS-CoV-2病毒中的特定蛋白質如何損害心臟組織(圖源:[1])
與未感染病毒的人相比,感染COVID-19的人在感染后至少一年內發生心肌炎癥、心律異常、血凝塊、中風、心臟病發作和心力衰竭的風險明顯更高。盡管科學家們迅速開發出疫苗和藥物來減輕COVID-19疾病的嚴重程度,但這些療法并不能保護心臟或其他器官免受即使是輕微感染也可能造成的損害。
“要長期治療患者,我們必須首先了解導致疾病的機制。我們的研究表明,單個的SARS-CoV-2蛋白質都可以對身體的特定組織造成重大損害,這與對其他病毒如艾滋病毒和寨卡病毒的發現類似,”高級作者、醫學教授、密歇根大學醫學院精確疾病建模中心主任Zhe Han博士說。“通過識別每個組織中的這些損傷過程,我們可以測試藥物,看看是否有任何藥物可以逆轉這種損傷;那些表現出希望的藥物可以在臨床研究研究中進一步測試。”
去年,Han博士和他的研究團隊在使用果蠅和人類細胞的研究中發現了毒性最強的SARS-CoV-2蛋白。他們發現了一種很有前途的藥物selinexor降低了其中一種蛋白質的毒性,但沒有降低另一種被稱為Nsp6的蛋白質的毒性。

圖2 遺傳篩選示意圖,通過心臟病理學識別特定的SARS-CoV-2基因(圖源:[1])
在他們最新的研究中,他們發現Nsp6是果蠅心臟中毒性最大的SARS-CoV-2蛋白。接下來,他們發現Nsp6蛋白質劫持了果蠅心臟中的細胞,啟動糖酵解過程,使細胞燃燒葡萄糖為能量。通常情況下,心臟細胞使用脂肪酸作為能量來源,但在心力衰竭時,這些細胞會轉換到糖代謝,試圖修復受損組織。研究人員還發現,Nsp6蛋白破壞了細胞的動力源——線粒體,線粒體通過糖代謝產生能量,從而增加了損傷。
然后,研究小組使用2-脫氧葡萄糖(2DG)阻斷果蠅和小鼠心臟細胞的糖代謝。他們發現這種藥物減少了由Nsp6病毒蛋白引起的心臟和線粒體損傷。

圖3 UAS-SARS-CoV-2Nsp6轉基因的4XH和Gal4、成纖維細胞特異性過表達(OE)誘導的成人心臟表型(圖源:[1])
“我們知道,一些病毒劫持受感染動物的細胞機制,改變其新陳代謝,竊取細胞的能量來源,所以我們懷疑SARS-CoV-2做了類似的事情。病毒還可以利用糖代謝的副產品作為制造更多病毒的基石,”Han博士說。“因此,我們預測這種將心臟新陳代謝改變到感染前的藥物對病毒是有害的,因為它既切斷了病毒的能量供應,也消除了病毒復制所需的片段。”
研究人員說,幸運的是,2DG很便宜,在實驗室研究中經常使用。盡管2DG尚未獲得美國食品和藥物管理局的批準用于治療疾病,但該藥物目前正在印度進行治療COVID-19的臨床試驗。
很多從COVID康復的美國人在幾周或幾個月后出現了危險的心臟疾病,我們需要了解發生這種情況的根本原因。隨著這項研究闡明了Nsp6蛋白的途徑,我們可以為未來的研究改進我們的治療目標,最終目標是逆轉這些患者的進一步心臟損傷。
參考資料:
[1] SARS-CoV-2 Nsp6 damages Drosophila heart and mouse cardiomyocytes through MGA/MAX complex-mediated increased glycolysis



