摘要:科學家們首次使用CRISPR技術插入基因,使免疫細胞集中攻擊癌細胞,有可能使正常細胞不受傷害,并提高免疫治療的有效性。
科學家首次使用CRISPR技術插入基因,使免疫細胞集中攻擊癌細胞,有可能使正常細胞不受傷害,并提高免疫治療的有效性。新方法在癌癥免疫治療學會(SITC) 2022上發表,并發表在《自然》雜志上。該研究由UCLA Jonsson綜合癌癥中心的Antoni Ribas醫學博士和UCLA醫學教授共同領導。

圖1 科學家首次使用CRISPR技術插入基因使免疫細胞集中攻擊癌細胞(圖源:[1])
CRISPR技術以前曾被用于去除人類的特定基因,使免疫系統更活躍地對抗癌癥。在這項新研究中,PACT制藥公司的研究人員報告稱,他們不僅能夠使用CRISPR去除特定基因,還能在免疫細胞中插入新的基因,有效地重新定向免疫細胞,識別患者自身癌細胞的突變。當注入回患者體內時,這些CRISPR工程免疫細胞優先流向癌細胞,并成為那里最有代表性的免疫細胞。
這項新研究報告了一種從患者自身血液中分離免疫受體的有效方法,使用的新技術最初是由Ribas博士與西雅圖系統生物學研究所所長James Heath博士、諾貝爾獎得主David Baltimore博士、加州理工學院名譽教授和UCLA Jonsson綜合癌癥中心成員合作開發的,并由PACT制藥公司進一步發展到臨床。分離后,利用CRISPR基因編輯,免疫受體被用于重定向免疫細胞來識別癌癥。
“這是在開發癌癥個性化治療方面的一個飛躍,在這種治療中,專門識別患者自身癌癥突變的免疫受體被用來治療癌癥。”該文章的通訊作者Ribas博士說。“如果沒有新開發的CRISPR技術一步取代臨床級細胞制劑中的免疫受體的能力,就不可能產生針對癌癥的個性化細胞治療方法。”
研究人員報告說,他們治療了16名患有各種實體癌癥的患者,包括結腸癌、乳腺癌和肺癌。根據結合情況,從患者的血液中分離出免疫細胞,以捕獲從患者自身癌癥中顯示出350個突變的試劑,針對免疫系統34種HLA亞型的總共超過5000個突變。讓免疫細胞特異性識別癌癥突變的免疫受體的基因被測序,總共有175個新分離的癌癥特異性免疫受體。然后,通過一步式CRISPR編輯,它們被插入到患者自身的免疫細胞中,這包括敲除現有的免疫細胞受體和敲入可以重定向這些細胞以專門識別癌癥突變的免疫受體。
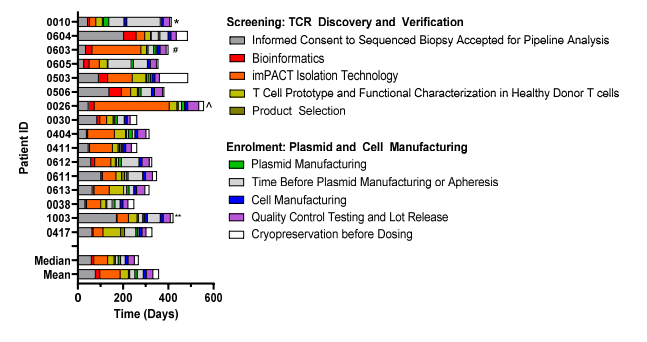
圖2 最終接受治療的14名患者篩選和給藥之間的時間線(圖源:[1])
在給予條件性化療后,多達三種這樣的基因編輯免疫細胞被注入回患者體內,參與這項研究的16名患者共被注入37種免疫受體。患者出現了化療的預期副作用,兩名患者出現了基因編輯細胞的潛在副作用,一名患者出現發燒和發冷,另一名患者出現精神錯亂,兩名患者都迅速康復。基因編輯的免疫細胞優先從患者輸注后的活組織檢查中恢復,通常代表癌癥中前20%的免疫細胞。
“這項研究證明了分離和克隆多個識別癌細胞突變的免疫細胞受體的可行性,使用單步、非病毒精確基因組編輯同時敲除內源性免疫受體和敲入重定向免疫受體的可行性,制造臨床級別的CRISPR工程T細胞,注入多達三種基因編輯免疫細胞產品的安全性,以及基因編輯的免疫細胞運輸到患者腫瘤的能力,”Ribas博士說。
參考資料:
[1] Non-viral precision T cell receptor replacement for personalized cell therapy
摘要:科學家們首次使用CRISPR技術插入基因,使免疫細胞集中攻擊癌細胞,有可能使正常細胞不受傷害,并提高免疫治療的有效性。
科學家首次使用CRISPR技術插入基因,使免疫細胞集中攻擊癌細胞,有可能使正常細胞不受傷害,并提高免疫治療的有效性。新方法在癌癥免疫治療學會(SITC) 2022上發表,并發表在《自然》雜志上。該研究由UCLA Jonsson綜合癌癥中心的Antoni Ribas醫學博士和UCLA醫學教授共同領導。

圖1 科學家首次使用CRISPR技術插入基因使免疫細胞集中攻擊癌細胞(圖源:[1])
CRISPR技術以前曾被用于去除人類的特定基因,使免疫系統更活躍地對抗癌癥。在這項新研究中,PACT制藥公司的研究人員報告稱,他們不僅能夠使用CRISPR去除特定基因,還能在免疫細胞中插入新的基因,有效地重新定向免疫細胞,識別患者自身癌細胞的突變。當注入回患者體內時,這些CRISPR工程免疫細胞優先流向癌細胞,并成為那里最有代表性的免疫細胞。
這項新研究報告了一種從患者自身血液中分離免疫受體的有效方法,使用的新技術最初是由Ribas博士與西雅圖系統生物學研究所所長James Heath博士、諾貝爾獎得主David Baltimore博士、加州理工學院名譽教授和UCLA Jonsson綜合癌癥中心成員合作開發的,并由PACT制藥公司進一步發展到臨床。分離后,利用CRISPR基因編輯,免疫受體被用于重定向免疫細胞來識別癌癥。
“這是在開發癌癥個性化治療方面的一個飛躍,在這種治療中,專門識別患者自身癌癥突變的免疫受體被用來治療癌癥。”該文章的通訊作者Ribas博士說。“如果沒有新開發的CRISPR技術一步取代臨床級細胞制劑中的免疫受體的能力,就不可能產生針對癌癥的個性化細胞治療方法。”
研究人員報告說,他們治療了16名患有各種實體癌癥的患者,包括結腸癌、乳腺癌和肺癌。根據結合情況,從患者的血液中分離出免疫細胞,以捕獲從患者自身癌癥中顯示出350個突變的試劑,針對免疫系統34種HLA亞型的總共超過5000個突變。讓免疫細胞特異性識別癌癥突變的免疫受體的基因被測序,總共有175個新分離的癌癥特異性免疫受體。然后,通過一步式CRISPR編輯,它們被插入到患者自身的免疫細胞中,這包括敲除現有的免疫細胞受體和敲入可以重定向這些細胞以專門識別癌癥突變的免疫受體。

圖2 最終接受治療的14名患者篩選和給藥之間的時間線(圖源:[1])
在給予條件性化療后,多達三種這樣的基因編輯免疫細胞被注入回患者體內,參與這項研究的16名患者共被注入37種免疫受體。患者出現了化療的預期副作用,兩名患者出現了基因編輯細胞的潛在副作用,一名患者出現發燒和發冷,另一名患者出現精神錯亂,兩名患者都迅速康復。基因編輯的免疫細胞優先從患者輸注后的活組織檢查中恢復,通常代表癌癥中前20%的免疫細胞。
“這項研究證明了分離和克隆多個識別癌細胞突變的免疫細胞受體的可行性,使用單步、非病毒精確基因組編輯同時敲除內源性免疫受體和敲入重定向免疫受體的可行性,制造臨床級別的CRISPR工程T細胞,注入多達三種基因編輯免疫細胞產品的安全性,以及基因編輯的免疫細胞運輸到患者腫瘤的能力,”Ribas博士說。
參考資料:
[1] Non-viral precision T cell receptor replacement for personalized cell therapy



