摘要:一項新的研究發現了一種蛋白質,這種蛋白質可以使黑色素瘤(最嚴重的皮膚癌類型)變得更具侵略性,因為它賦予癌細胞改變細胞核形狀的能力——這種特征允許細胞在身體各處遷移和擴散。
倫敦瑪麗女王大學、倫敦國王學院和弗朗西斯克里克研究所領導的研究發現了一種蛋白質,這種蛋白質通過賦予癌細胞改變細胞核形狀的能力,使黑色素瘤(最嚴重的皮膚癌類型)更具攻擊性,這種特征使細胞能夠在全身遷移和擴散。
發表在《自然細胞生物學》雜志上的這項研究,模擬了侵襲性黑色素瘤細胞的行為,這種細胞能夠改變細胞核的形狀,克服癌細胞在組織中遷移時遇到的物理限制。研究發現,這些侵襲性黑素瘤細胞中含有一種叫做LAP1的蛋白質,這種蛋白質水平的升高與黑素瘤患者預后不良有關。

圖1 研究發現LAP1蛋白質的升高與黑素瘤患者預后不良有關(圖源:[1])
黑色素瘤是一種皮膚癌,可以擴散到身體的其他器官。癌癥擴散或“轉移”是癌癥相關死亡的主要原因。雖然轉移已被廣泛研究,但其發生機制尚不清楚。這項研究的發現為黑色素瘤的發展機制提供了新的線索,并可能為開發針對黑色素瘤擴散的新方法鋪平道路。
通過細胞核遷移
該研究由巴茨癌癥研究所的Victoria Sanz-Moreno教授和倫敦國王學院及弗朗西斯-克里克研究所的Jeremy Carlton博士共同領導,主要由英國癌癥研究中心、惠康基金會和巴茨慈善機構資助。
在這項研究中,研究小組在實驗中挑戰侵襲性和非侵襲性黑素瘤細胞,讓它們通過比細胞核尺寸小的人造膜上的孔隙遷移。侵襲性細胞來自一名黑色素瘤患者的轉移部位,而侵襲性較低的細胞來自同一名患者的原始或“原發性”黑色素瘤。
為了轉移,癌細胞需要從原發腫瘤中分離出來,轉移到身體的另一部分并在那里開始生長。然而,腫瘤周圍的致密環境使癌細胞很難在物理上進行這種操作。
細胞包含一個大而堅硬的結構,稱為細胞核,它存儲細胞的遺傳信息,但它也限制了細胞通過腫瘤環境中緊密間隙的能力。為了讓癌細胞擠過這些縫隙,它們需要讓細胞核更具延展性。
遷移實驗后進行的成像顯示,具有侵襲性的細胞能夠比侵襲性較低的細胞更有效地通過孔隙,因為它們在細胞核邊緣形成了稱為“"blebs(核膜泡,生物通注)”的凸起。對黑色素瘤細胞的遺傳分析顯示,形成泡狀物的侵襲性細胞含有更高水平的LAP1蛋白,這種蛋白位于圍繞細胞核的膜(稱為核膜)內。
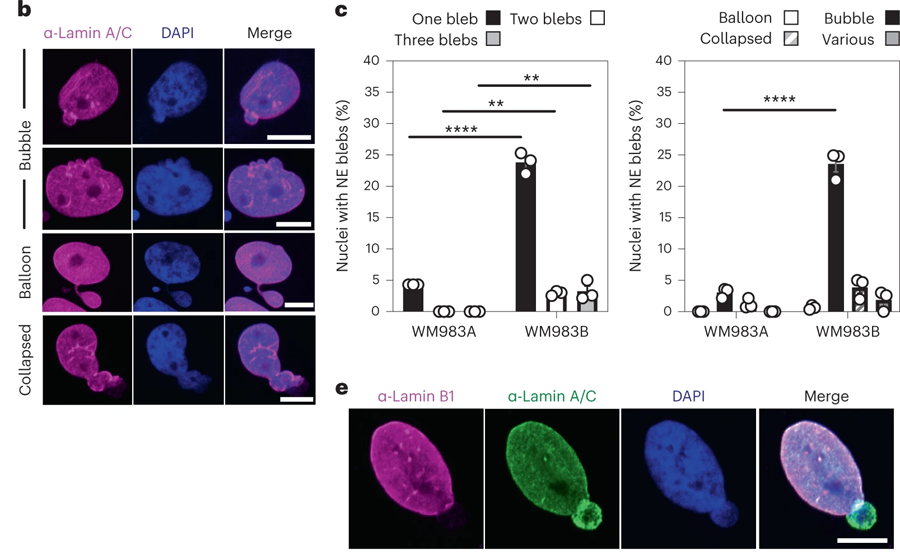
圖2 轉移性黑色素瘤細胞的NE(核包膜蛋白)是高度活躍的(圖源:[1])
Jeremy Carlton博士的實驗室對理解細胞內膜結合結構的動力學很感興趣,他說:
“核膜被拴在下面的細胞核上,我們的研究表明,LAP1蛋白松開了這種束縛,使核膜隆起并形成氣泡,使細胞核更流動。因此,癌細胞可以擠過通常會阻止它們的縫隙。”
當研究小組在實驗中阻斷了侵襲性細胞中LAP1蛋白的產生,然后再讓癌細胞通過小孔時,他們發現細胞形成核膜泡的能力較弱,也較難擠過這些空隙。
研究小組還在患者的黑色素瘤樣本中觀察到相同的LAP1表達模式。與原發腫瘤相比,從黑色素瘤患者轉移部位提取的組織樣本中LAP1水平更高。在原發腫瘤邊緣的細胞中有高水平LAP1的患者具有更強的侵襲性癌癥和更差的結果,這表明這種蛋白質可以用來識別可能具有更高侵襲性疾病風險的黑色素瘤患者亞群。
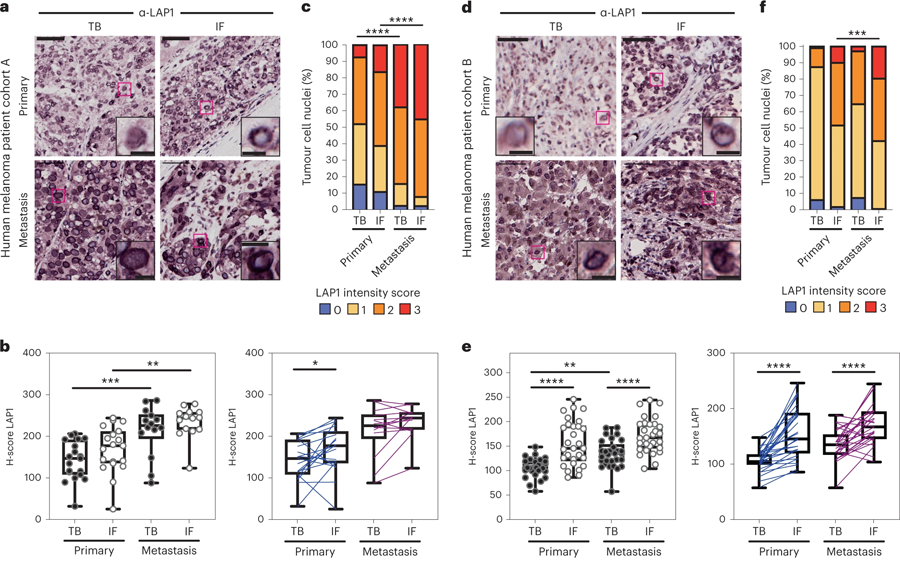
圖3 LAP1水平在人類黑色素瘤進展中增加(圖源:[1])
Sanz-Moreno教授的研究小組對了解癌細胞如何與環境溝通以促進其生長和擴散感興趣,他說:
黑素瘤是最具侵略性和最致命的皮膚癌類型。通過結合我的實驗室和Carlton博士的專業知識,我們對LAP1如何促進黑色素瘤進展有了新的機制理解,并在實驗室和患者模型中證明了LAP1是黑色素瘤侵襲性的關鍵調節因子。”
“因為LAP1在轉移細胞中表達如此之高,干擾這一分子機制可能會對癌癥擴散產生重大影響。目前還沒有直接靶向LAP1的藥物,所以展望未來,我們希望研究靶向LAP1和核膜泡的方法,看看是否有可能阻止黑色素瘤的發展機制。”
研究小組希望研究LAP1驅動的核膜起泡是否發生在其他組成并穿過腫瘤環境的細胞(如免疫細胞)中,確定其他細胞中的這一過程是否有助于或阻礙癌癥的進展。
Iain Foulkes博士是英國癌癥研究所研究與創新的執行主任,該研究所為這項研究提供了部分資金,他說:
“像這樣的研究是一個很好的例子,說明了為什么英國癌癥研究中心熱衷于資助研究,除了關注臨床研究之外,還會進一步了解癌癥對我們身體生物學的影響。”
這種對黑素瘤細胞核如何變得更有流動性,能在體內移動的新認識,有助于建立我們對癌癥如何運作的認識,并為研究如何使癌癥更難擴散開辟了新的途徑。”
參考資料:
[1] Jung-Garcia, Y., Maiques, O., Monger, J. et al. LAP1 supports nuclear adaptability during constrained melanoma cell migration and invasion. Nat Cell Biol, 2023 DOI: 10.1038/s41556-022-01042-3
摘要:一項新的研究發現了一種蛋白質,這種蛋白質可以使黑色素瘤(最嚴重的皮膚癌類型)變得更具侵略性,因為它賦予癌細胞改變細胞核形狀的能力——這種特征允許細胞在身體各處遷移和擴散。
倫敦瑪麗女王大學、倫敦國王學院和弗朗西斯克里克研究所領導的研究發現了一種蛋白質,這種蛋白質通過賦予癌細胞改變細胞核形狀的能力,使黑色素瘤(最嚴重的皮膚癌類型)更具攻擊性,這種特征使細胞能夠在全身遷移和擴散。
發表在《自然細胞生物學》雜志上的這項研究,模擬了侵襲性黑色素瘤細胞的行為,這種細胞能夠改變細胞核的形狀,克服癌細胞在組織中遷移時遇到的物理限制。研究發現,這些侵襲性黑素瘤細胞中含有一種叫做LAP1的蛋白質,這種蛋白質水平的升高與黑素瘤患者預后不良有關。

圖1 研究發現LAP1蛋白質的升高與黑素瘤患者預后不良有關(圖源:[1])
黑色素瘤是一種皮膚癌,可以擴散到身體的其他器官。癌癥擴散或“轉移”是癌癥相關死亡的主要原因。雖然轉移已被廣泛研究,但其發生機制尚不清楚。這項研究的發現為黑色素瘤的發展機制提供了新的線索,并可能為開發針對黑色素瘤擴散的新方法鋪平道路。
通過細胞核遷移
該研究由巴茨癌癥研究所的Victoria Sanz-Moreno教授和倫敦國王學院及弗朗西斯-克里克研究所的Jeremy Carlton博士共同領導,主要由英國癌癥研究中心、惠康基金會和巴茨慈善機構資助。
在這項研究中,研究小組在實驗中挑戰侵襲性和非侵襲性黑素瘤細胞,讓它們通過比細胞核尺寸小的人造膜上的孔隙遷移。侵襲性細胞來自一名黑色素瘤患者的轉移部位,而侵襲性較低的細胞來自同一名患者的原始或“原發性”黑色素瘤。
為了轉移,癌細胞需要從原發腫瘤中分離出來,轉移到身體的另一部分并在那里開始生長。然而,腫瘤周圍的致密環境使癌細胞很難在物理上進行這種操作。
細胞包含一個大而堅硬的結構,稱為細胞核,它存儲細胞的遺傳信息,但它也限制了細胞通過腫瘤環境中緊密間隙的能力。為了讓癌細胞擠過這些縫隙,它們需要讓細胞核更具延展性。
遷移實驗后進行的成像顯示,具有侵襲性的細胞能夠比侵襲性較低的細胞更有效地通過孔隙,因為它們在細胞核邊緣形成了稱為“"blebs(核膜泡,生物通注)”的凸起。對黑色素瘤細胞的遺傳分析顯示,形成泡狀物的侵襲性細胞含有更高水平的LAP1蛋白,這種蛋白位于圍繞細胞核的膜(稱為核膜)內。

圖2 轉移性黑色素瘤細胞的NE(核包膜蛋白)是高度活躍的(圖源:[1])
Jeremy Carlton博士的實驗室對理解細胞內膜結合結構的動力學很感興趣,他說:
“核膜被拴在下面的細胞核上,我們的研究表明,LAP1蛋白松開了這種束縛,使核膜隆起并形成氣泡,使細胞核更流動。因此,癌細胞可以擠過通常會阻止它們的縫隙。”
當研究小組在實驗中阻斷了侵襲性細胞中LAP1蛋白的產生,然后再讓癌細胞通過小孔時,他們發現細胞形成核膜泡的能力較弱,也較難擠過這些空隙。
研究小組還在患者的黑色素瘤樣本中觀察到相同的LAP1表達模式。與原發腫瘤相比,從黑色素瘤患者轉移部位提取的組織樣本中LAP1水平更高。在原發腫瘤邊緣的細胞中有高水平LAP1的患者具有更強的侵襲性癌癥和更差的結果,這表明這種蛋白質可以用來識別可能具有更高侵襲性疾病風險的黑色素瘤患者亞群。

圖3 LAP1水平在人類黑色素瘤進展中增加(圖源:[1])
Sanz-Moreno教授的研究小組對了解癌細胞如何與環境溝通以促進其生長和擴散感興趣,他說:
黑素瘤是最具侵略性和最致命的皮膚癌類型。通過結合我的實驗室和Carlton博士的專業知識,我們對LAP1如何促進黑色素瘤進展有了新的機制理解,并在實驗室和患者模型中證明了LAP1是黑色素瘤侵襲性的關鍵調節因子。”
“因為LAP1在轉移細胞中表達如此之高,干擾這一分子機制可能會對癌癥擴散產生重大影響。目前還沒有直接靶向LAP1的藥物,所以展望未來,我們希望研究靶向LAP1和核膜泡的方法,看看是否有可能阻止黑色素瘤的發展機制。”
研究小組希望研究LAP1驅動的核膜起泡是否發生在其他組成并穿過腫瘤環境的細胞(如免疫細胞)中,確定其他細胞中的這一過程是否有助于或阻礙癌癥的進展。
Iain Foulkes博士是英國癌癥研究所研究與創新的執行主任,該研究所為這項研究提供了部分資金,他說:
“像這樣的研究是一個很好的例子,說明了為什么英國癌癥研究中心熱衷于資助研究,除了關注臨床研究之外,還會進一步了解癌癥對我們身體生物學的影響。”
這種對黑素瘤細胞核如何變得更有流動性,能在體內移動的新認識,有助于建立我們對癌癥如何運作的認識,并為研究如何使癌癥更難擴散開辟了新的途徑。”
參考資料:
[1] Jung-Garcia, Y., Maiques, O., Monger, J. et al. LAP1 supports nuclear adaptability during constrained melanoma cell migration and invasion. Nat Cell Biol, 2023 DOI: 10.1038/s41556-022-01042-3



